Mempunyai unsur yang berkutub dan berkutub kalau non polar. Contoh molekul polar meliputi.

Percobaan Senyawa Polar Dan Non Polar
Contoh senyawa non polar. Perhatikan senyawa ionik seperti natrium klorida nacl bersifat polar. Jika perbedaan elektronegativitas antara atom lebih besar dari 20 ikatannya bersifat ionik. Contoh pelarut non polar yaitu. Pelarut non polar mengandung ikatan dengan atom elektronegatif yang sama seperti c dan h. Senyawa ionik adalah molekul yang sangat polar. Cl2 pcl5 h2 n2.
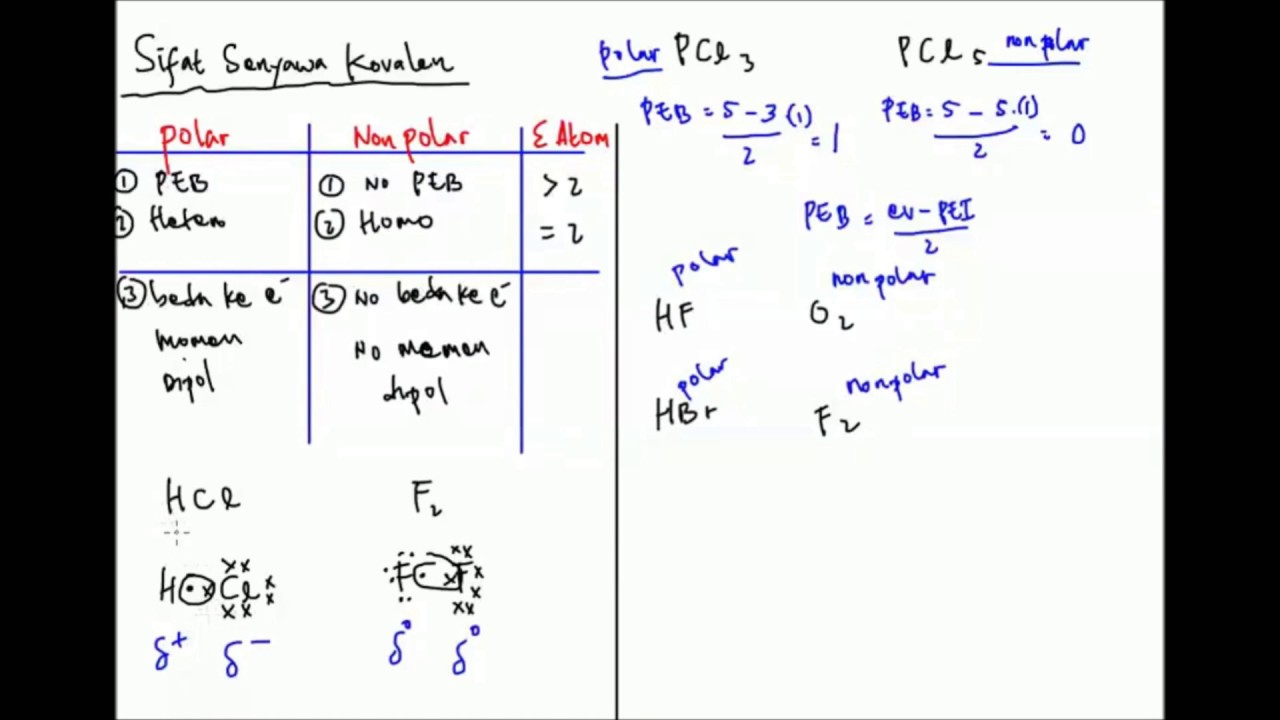
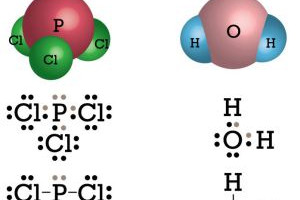
Contoh senyawa lain yang memiliki bentuk molekul simetris dan bersifat nonpolar adalah ch 4 bh 3 bcl 3 pcl 5 dan co 2. Senyawa polar dan non polar pengertian ciri kovalen perbedaan sifat titik didih contoh. Dalam hal ini untuk dapat membedakan kedua senyawa berikut ini yakni senyawa polar dan non polar yang dapat ditunjukan dari beberapa sisi yang diantaranya dari ciri senyawa distribusi elektronnya dan ukuran kuantitatif titik didih. Untuk dapat menentukan senyawa tersebut termasuk senyawa polar atau nonpolar kita harus mengetahui struktur lewis nya terlebih dahulu. Susunan elekronnya simetris 3. Mempunyai atom yang elektronegatif tinggi seperti golongan 567 3.
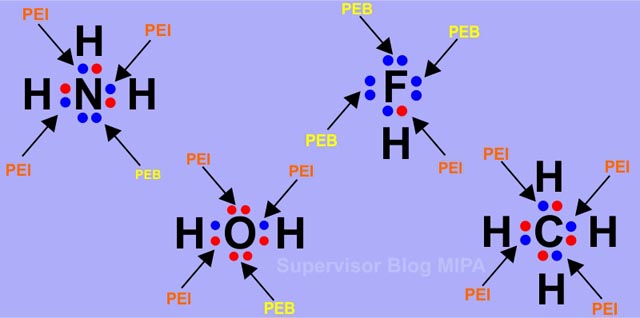
Sususnan elektronnya asimetris 4. Lihat juga materi kimia lainnya. Mempunyai peb diatom pusat 2. Ikatan antara 8 o dengan 8 o. Air h2o amonia nh3 belerang dioksida so2 hidrogen sulfida h2s etanol c2h6o. Tidak ada peb diatom pusat 2.
Atomnya harus berbeda 5. Perhatikan struktur salah satu ikatan kovalen non polar dari ch 4 berikut. Ciri ciri senyawa polar dan non polar adalah. Ini terdiri dari molekul non polar dan dapat melarutkan senyawa atau zat terlarut non polar. Ok mari kita kerjakan.